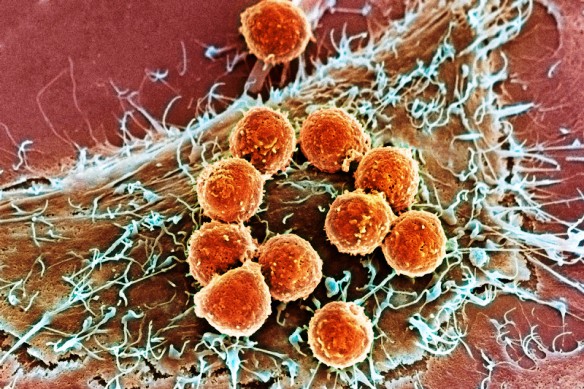
ΚΑΡΚΙΝΟΣ ΑΙΤΙΑ
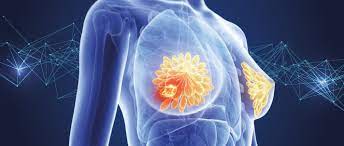
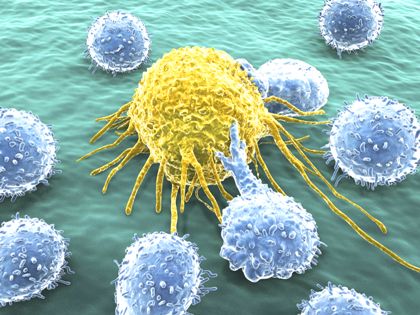
(Στη φωτογραφία φαίνεται καρκινικό κύτταρο του τραχήλου)
Ενημερώθηκε στις 19/8/2023
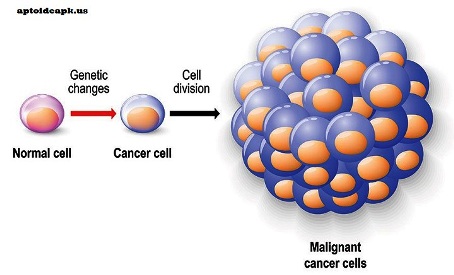
Ο Καρκίνος (οι καρκίνοι) είναι ομάδα παθήσεων οι οποίες χαρακτηρίζονται από αχρείαστο και ανεξέλεγκτο πολλαπλασιασμό παθολογικών κυττάρων που εξαπλώνονται και καταστρέφουν γειτονικούς και απομακρυσμένους φυσιολογικούς ιστούς προκαλώντας τελικά το θάνατο, αν δεν αντιμετωπιστεί.
[Ενώ οι διαιρέσεις και ο προγραμματισμένος θάνατος στα φυσιολογικά κύτταρα του σώματος είναι αυστηρά ελεγχόμενα από το DNA μας, με πολλές δικλείδες ασφαλείας]
Ο καρκίνος (ή κακοήθης όγκος) έχει τη δυνατότητα για εισβολή σε γειτονικές περιοχές και σε τοπικούς λεμφαδένες μέσω των λεμφαγγείων και διασκορπισμό σε άλλες απομακρυσμένες περιοχές του σώματος, μέσω του αίματος (μετάσταση), ενώ ο καλοήθης όγκος παραμένει τοπικός.
[Οι μεταστάσεις (μεταστατικοί όγκοι) στις περισσότερες περιπτώσεις βρίσκονται στον πνεύμονα, στο ήπαρ, τον εγκέφαλο και τα οστά.]
Ο καρκίνος παρουσιάζει περίπου 200 διαφορετικούς τύπους, ανάλογα με τον ιστό που βρίσκονται και ξεκινούν από ένα μόνο κύτταρο, που απέκτησε καρκινικές ιδιότητες συνήθως σε διάστημα χρόνων ή και δεκαετιών.
Οι συχνότεροι καρκίνοι είναι στον πνεύμονα, στο μαστό, στον προστάτη, στο παχύ έντερο, στο στομάχι, στο δέρμα.
(Η θεραπεία του καρκίνου φαίνεται σε άλλο άρθρο)
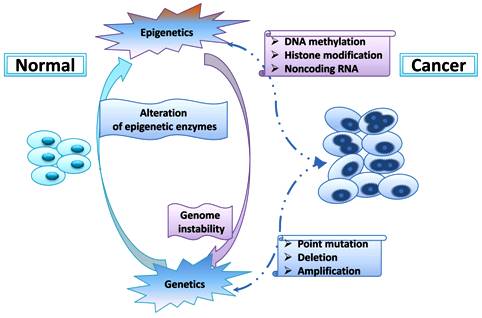
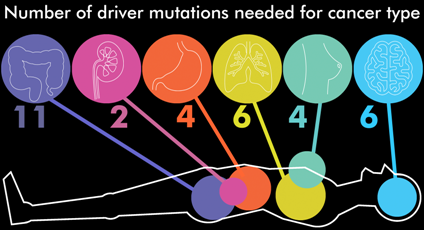
>> Οι Καρκίνοι προκαλούνται από διάφορες αιτίες που έχουν σαν αποτέλεσμα μεταλλάξεις σε συγκεκριμένα γονίδια που ευνοούν τον καρκίνο ή/και επιγενετικές αλλαγές σ’ αυτά τα γονίδια.
[Οι επιγενετικές αλλαγές ενεργοποιούν ή απενεργοποιούν γονίδια που σχετίζονται με τον καρκίνο μέσω ενεργοποίησης ή απενεργοποίησης της δημιουργίας mRNA από αυτά]
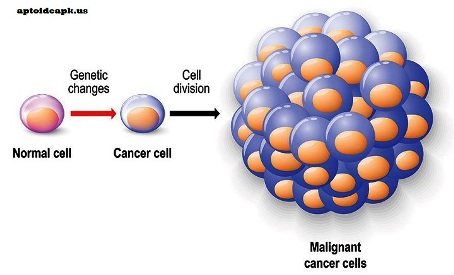
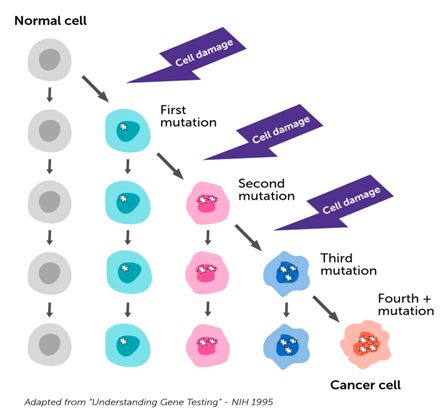
> Η συσσώρευση μεταλλάξεων ή/και επιγενετικών αλλαγών διαρκεί συνήθως χρόνια ώστε να δημιουργηθεί το πρώτο καρκινικό κύτταρο.
>>> Το πρώτο καρκινικό κύτταρο έχει καταφέρει να ξεφύγει διαδοχικά από όλους τους ελέγχους και επιδιορθώσεις του DNA (κατά τις κυτταρικές διαιρέσεις και τις βλάβες του από άλλους παράγοντες), από τον προγραμματισμένο θάνατο (απόπτωση) όσων κυττάρων δημιουργηθούν με ελαττωματικό DNA και επιπλέον καταφέρνει να “κρυφτεί” από το ανοσοποιητικό σύστημα για να μην εξοντωθεί.
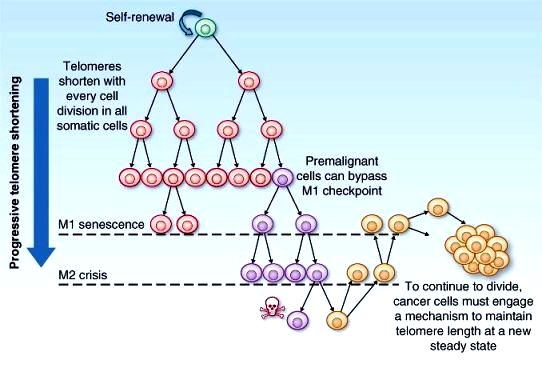
>> Στη συνέχεια αυτό βρίσκει τρόπο να διαιρείται χωρίς ελέγχους, αμέτρητες φορές (με διατήρηση του μήκος των τελομερών στο ελάχιστο δυνατό). Δες πιο κάτω
Η ΔΗΜΙΟΥΡΓΙΑ ΤΟΥ ΚΑΡΚΙΝΟΥ
Για τη δημιουργία του καρκινικού κυττάρου είναι απαραίτητες:
α) Αρχικά οι κατάλληλες διαδοχικές μεταλλάξεις σε πολλά γονίδια που ευνοούν τον καρκίνο ή/και οι επιγενετικές αλλαγές, που ενεργοποιούν ή απενεργοποιούν γονίδια που ευνοούν τον καρκίνο.
>> Οι μεταλλάξεις ή/και οι επιγενετικές αλλαγές, γίνονται σε τρία είδη γονιδίων:
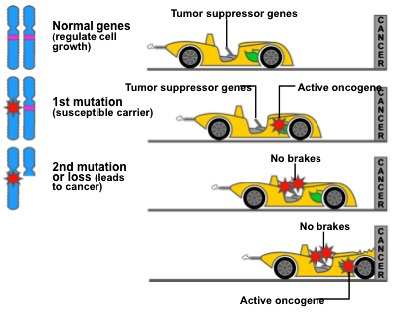
α) στα ογκογονίδια που αυξάνεται η δράση τους (αυτά αυξάνουν τις κυτταρικές διαιρέσεις π.χ. γονίδια της οικογένειας ras). Αυτά δημιουργούνται από τα πρωτο-ογκογονίδια και παρομοιάζονται με το πεντάλ της βενζίνης στο αυτοκίνητο (αυτοκίνητο εννοούμε τις κυτταρικές διαιρέσεις).
β) σε γονίδια που καταπιέζουν τη δημιουργία όγκων που μειώνεται η δράση τους. αυτά παρομοιάζονται με το πεντάλ του φρένου στο αυτοκίνητο.
γ) σε γονίδια που διορθώνουν το DNA που μειώνεται η δράση τους. Αυτά διορθώνουν το DNA από τις συνεχείς βλάβες του κατά τις διαιρέσεις των κυττάρων, και τις περιβαλλοντικές μεταλλάξεις. Αυτά παρομοιάζονται με συνεργείο επισκευής των βλαβών του αυτοκινήτου.
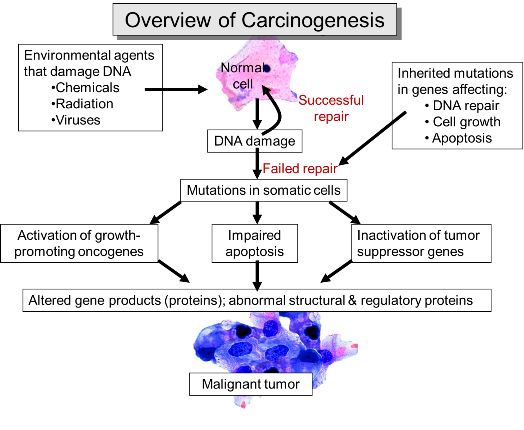
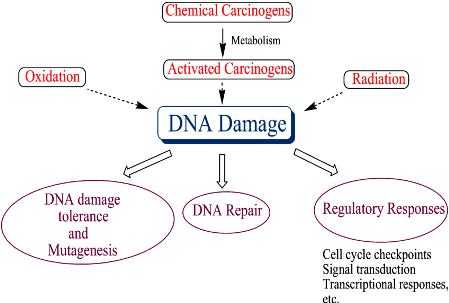
>> Οι μεταλλάξεις δημιουργούνται από βλάβες στο DNA είτε τυχαία (σποραδικά) είτε από ενδογενείς παράγοντες (π.χ. από μεγάλη ηλικία), είτε μεταφέρονται κληρονομικά (περίπου 7% των καρκίνων). (Δες πιο κάτω)
>> Το DNA μας υφίσταται συνεχείς βλάβες τόσο από ενδογενείς παράγοντες (π.χ. από λάθη αντιγραφής του DNA, από τη δημιουργία ελεύθερων ριζών Οξυγόνου ή ROS ) όσο και από εξωγενείς παράγοντες π.χ. υπεριώδη ηλιακή ακτινοβολία, άλλα είδη ακτινοβολίας, το κάπνισμα, ορισμένες τοξίνες, ορισμένες χημικές αρωματικές ουσίες όπως το βενζόλιο και το τολουένιο, από ιώσεις κλπ. (Δες στο τέλος)
[Κάποια κληρονομικότητα υπάρχει και στους σποραδικούς καρκίνους, όπου αν πρώτου βαθμού συγγενής έχει παρουσιάσει καρκίνο, υπάρχει περίπου 2πλάσια πιθανότητα να εμφανιστεί καρκίνος, συγκριτικά με τους άλλους ανθρώπους]
>> Επιγενετικά οι βλάβες στο DNA και συνεπώς ο καρκίνος δημιουργείται από περιβαλλοντικούς παράγοντες και από βλαβερές υγεινοδιαιτητικές συνήθειες.
Αυτά είναι: Το κάπνισμα (περίπου 22% των περιπτώσεων), η παχυσαρκία, η καθιστική ζωή και η κακή διατροφή (αθροιστικά περίπου 25% των περιπτώσεων), η κατανάλωση οινοπνευματωδών (περίπου 6% των περιπτώσεων), οι λοιμώξεις κυρίως από ογκο-ιούς (περίπου 10-15% των περιπτώσεων) ή από μικρόβια (π.χ. ελικοβακτηρίδιο του πυλωρού), η ακτινοβολία (όλων των ειδών), η μόλυνση του αέρα, η ηλιοθεραπεία, ορισμένα χημικά στη διατροφή, εντομοκτόνα, από βλαβερό περιβάλλον εργασίας (π.χ. η έκθεση σε βενζόλιο μπορεί να προκαλέσει λευχαιμία) ή κατοικίας (π.χ. συνεχής έκθεση σε ραδόνιο) κλπ.
>> Επιπλέον ορισμένα φάρμακα, αυξάνουν τον κίνδυνο μελλοντικού καρκίνου, όπως αυτά που προκαλούν μείωση της δράσης του ανοσοποιητικού συστήματος, ορισμένες ορμόνες, και ορισμένα χημειοθεραπευτικά του καρκίνου.
>> Επίσης η χρόνια φλεγμονή (π.χ. καρκίνος παχέως εντέρου) και η διέγερση από ορμόνες (π.χ. καρκίνος μαστού, ενδομητρίου, προστάτη, θυρεοειδούς κλπ.) ευνοούν τη δημιουργία καρκίνου και το μικροβίωμα διαφόρων ιστών (π.χ. παχέως εντέρου, δέρματος, κόλπου κλπ.) ίσως συμμετέχει στη δημιουργία καρκίνου, ιδίως στον καρκίνο του παχέως εντέρου.
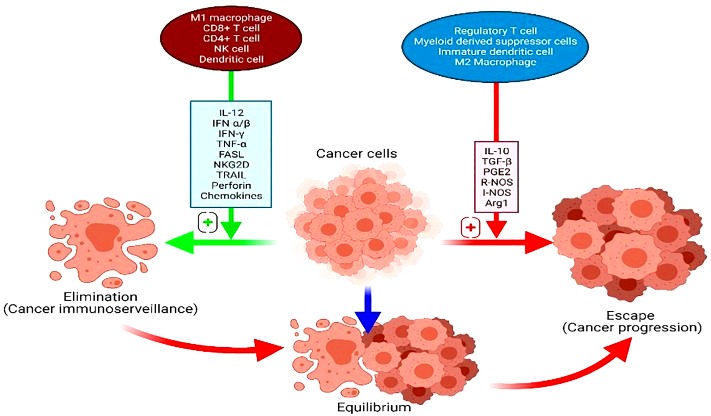
>>> Οι αντικαρκινικοί μηχανισμοί του σώματος μας που καταπιέζουν τη δημιουργία όγκων είναι: Τα γονίδια που εμποδίζουν τον καρκίνο (tumor suppressor genes), τα γονίδια που επιδιορθώνουν το DNA, και “μικρά” RNAs (miRNAs) που εμποδίζουν τον καρκίνο και λέγονται tumor suppressor miRs.
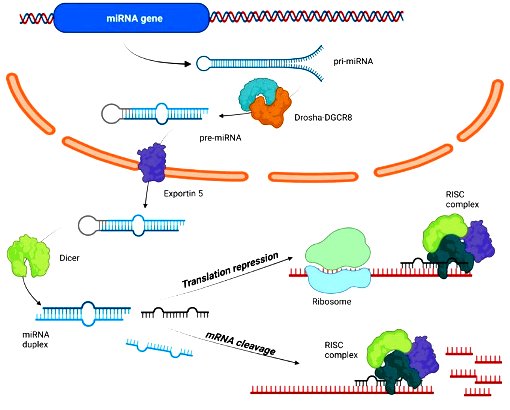
[Τα miRNAs είναι μικρά RNAs, που δημιουργούνται από γονίδια miRNA (noncoding genes). Αυτά δεν προκαλούν παραγωγή πρωτεΐνης αλλά μειώνουν την παραγωγή πρωτεΐνης από κάποιο άλλα γονίδιο απενεργοποιώντας mRNA του γονιδίου αυτού] Δες στο τέλος
[Παράδειγμα γονιδίου που καταπιέζει τη δημιουργία όγκων είναι το γονίδιο tp53 που θεωρείται ο φύλακας άγγελος του DNA, μειώνοντας τις αχρείαστες κυτταρικές διαιρέσεις και προκαλώντας θάνατο στα κύτταρα με ελαττωματικό DNA.
Τα tumor suppressor miRs μειώνουν τη δημιουργία πρωτεϊνών από τα ογκογονίδια, έτσι όταν αυξηθεί η έκφραση τους (η “δράση” τους), μειώνεται η καρκινογένεση]
>>> Οι μηχανισμοί που ευνοούν τον καρκίνο δημιουργούνται από τα Ογκογονίδια και τα oncomiRs.
[Τα Ογκογονίδια αυξάνουν τις κυτταρικές διαιρέσεις και μειώνουν τον προγραμματισμένο θάνατο των κυττάρων, ενώ τα oncomiRs μειώνουν τη δράση γονιδίων που καταπιέζουν τη δημιουργία όγκων, γονιδίων που επιδιορθώνουν το DNA και γονιδίων που προκαλούν προγραμματισμένο θάνατο. (Δες στο τέλος)]
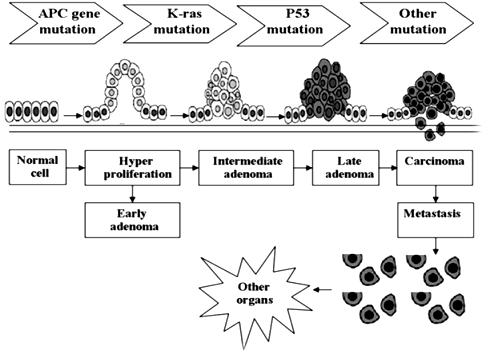
Πιο πάνω φαίνεται πως διαδοχικές μεταλλάξεις γονιδίων προκαλούν πολύποδα (αδένωμα) και τελικά καρκίνο στο παχύ έντερο (το APC και το Ρ53 είναι γονίδια που καταπιέζουν τη δημιουργία όγκων / Το Κ ras είναι ογκογονίδιο).
https://www.youtube.com/watch?v=UlHK3Y_c5Wo
β) Στη συνέχεια αφού καταφέρει να ξεφύγει από τον προγραμματισμένο θάνατο (απόπτωση), το πρώτο καρκινικό κύτταρο πρέπει να αρχίσει να διαιρείται.
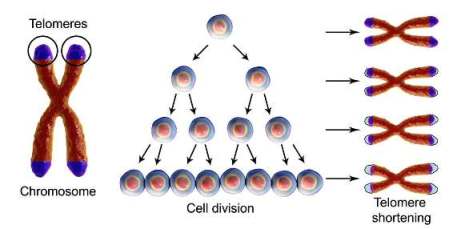
Για να συμβεί αυτό τα καρκινικά κύτταρα κυρίως διατηρούν το μήκος των τελομερών τους στο ελάχιστο δυνατό για να μπορούν να συνεχίζουν τις διαιρέσεις, οπότε γίνονται “αθάνατα” (με αμέτρητες διαιρέσεις).
[Τα τελομερή είναι ειδικοί προστατευτικοί σχηματισμοί που “σφραγίζουν” τις δυο άκρες των χρωματοσωμάτων για να προστατεύσουν το DNA από τη φθορά, που συμβαίνει κυρίως κατά τις κυτταρικές διαιρέσεις.
Αυτά θυσιάζονται – καταστρέφονται μερικώς για να μην καταστραφούν τα χρήσιμα γονίδια κατά τον αυτοδιπλασιασμό του DNA στις κυτταρικές διαιρέσεις.
Τα κύτταρα μας έχουν όριο ζωής, όμως για να ζούμε μέχρι τα γεράματα τα περισσότερα κύτταρα μας υφίστανται περίπου 40- 70 διαιρέσεις – ανανεώσεις.
Όταν φτάσουμε στο ανώτατο όριο διαιρέσεων σε κάθε είδος κύτταρο, τα τελομερή έχουν μικρύνει τόσο πολύ που τα κύτταρα δεν μπορούν να ανανεωθούν άλλο, οπότε φτάνουμε στη γήρανση του κυττάρου και τελικά στο θάνατο του.
Υπ’ όψιν ότι δεν έχουμε όλοι οι άνθρωποι το ίδιο μήκος τελομερών γιατί αυτό καθορίζεται εν μέρει κληρονομικά και εν μέρει επιγενετικά (από εξωγενείς αιτίες)]
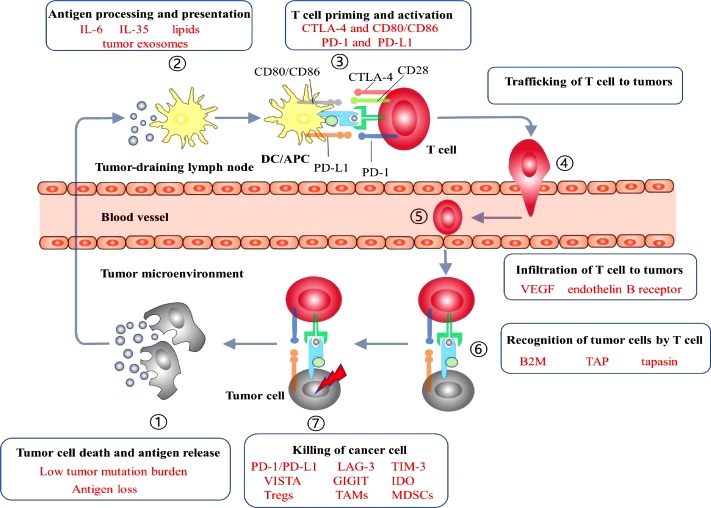
γ) Επιπλέον τα καρκινικά κύτταρα πρέπει να καταφέρουν να ΜΗ δέχονται επιθέσεις από το ανοσοποιητικό σύστημα και πιθανώς το καταφέρνουν προκαλώντας δυσλειτουργία στα Δεντριτικά κύτταρα και επιπλέον προκαλώντας ανοσοκατασταλτικό μικροπεριβάλλον γύρω τους (προκαλούν περιφερική ανοσολογική ανοχή).
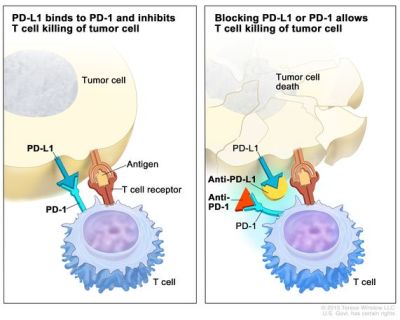
[Μερικοί καρκίνοι για να αποφύγουν την εξόντωση, ενεργοποιούν την checkpoint πρωτεΐνη PD-1.
Η πρωτεΐνη PD-1 εμποδίζει το ανοσοποιητικό να επιτίθεται εναντίον των δικών μας φυσιολογικών κυττάρων. Το επιτυγχάνει με αύξηση της ανοσολογικής ανοχής, μέσω αύξησης των Τ reg Λεμφοκυττάρων και μείωσης της δράσης των Τ Λεμφοκυττάρων (CD4+, CD8+).
Η δυσλειτουργία στα Δεντριτικά κύτταρα και τα άλλα αντιγονοπαρουσιαστικά κύτταρα (π.χ. Μακροφάγα, Β λεμφοκύτταρα) έχει σαν αποτέλεσμα να μη δημιουργούνται δραστικά CD4+ και CD8+ Τ Λεμφοκύτταρα (από τα αντίστοιχα παρθένα Τ Λεμφοκύτταρα).]
Στην εικόνα φαίνεται καρκινικό κύτταρο που δέχεται επίθεση από κυτταροτοξικά CD8+ Τ λεμφοκύτταρα.
https://www.sciencedirect.com/science/article/pii/S0306987721001821
https://www.sciencedirect.com/science/article/pii/S1567576920311140
δ) Όσον αφορά τους συμπαγείς όγκους, ο καρκίνος πρέπει να δημιουργήσει και νέα αγγεία για να τραφούν τα κύτταρα του.
[Όσες περισσότερες διαιρέσεις υφίστανται τα ενήλικα σωματικά κύτταρα και τα βλαστοκύτταρα, τόσο περισσότερες μεταλλάξεις αθροίζονται σ’ αυτά λόγω αναπόφευκτων λαθών στην αντιγραφή του DNA, οπότε αυξάνεται ο κίνδυνος καρκίνου.
Σχεδόν όλα τα κύτταρα στο σώμα μας ανανεώνονται συνεχώς (γιατί γερνούν και πεθαίνουν), είτε μέσω διαιρέσεων τους είτε από τα σωματικά βλαστοκύτταρα, ανάλογα με τον ιστό που βρίσκονται και ανάλογα με τις συνθήκες.
Στις κυτταρικές διαιρέσεις μεταφέρεται ακριβώς το ίδιο, αρχικό, γονιδιακό υλικό (DNA) του πρώτου κυττάρου (γονιμοποιημένου ωαρίου) από τη μια γενιά κυττάρων στις επόμενες γενιές, ενώ τα καρκινικά κύτταρα έχουν μεταλλαγμένο DNA που μεταφέρεται στις επόμενες γενιές κυττάρων, αλλά δεν μεταφέρεται στους απογόνους.]
>> Σύντομα αναμένεται να ανιχνεύονται ακριβώς οι “βλάβες” των γονιδίων που οδήγησαν στον καρκίνο και έτσι αυτός να αντιμετωπίζεται σε κάθε άνθρωπο με εξατομικευμένες και στοχευμένες θεραπείες (personalized targeted therapies).
ΟΙ ΔΙΑΙΡΕΣΕΙΣ ΤΩΝ ΚΑΡΚΙΝΙΚΩΝ ΚΥΤΤΑΡΩΝ
Το αρχικό καρκινικό κύτταρο διαιρείται σε 2 θυγατρικά, αυτά σε 4 και έτσι συνεχώς διπλασιάζεται ο αριθμός τους, έτσι μετά από 30 κύκλους διαιρέσεων ο αριθμός των καρκινικών κυττάρων φτάνει στο 1 δισεκατομμύριο, ζυγίζουν περίπου 1 γραμμάριο και καταλαμβάνουν χώρο περίπου ενός κυβικού εκατοστού.
Στην ανωτέρω εικόνα φαίνεται καρκινικό κύτταρο του μαστού τη “στιγμή” της διαίρεσης του
Το πρώτο καρκινικό κύτταρο αρχίζει να πολλαπλασιάζεται συνεχώς κυρίως μέσω αύξησης της τελομεράσης (ή στο 10% από άλλους μηχανισμούς σταθεροποίησης του μήκους των τελομερών, που λέγονται ALT).
ΓΕΝΙΚΑ ΓΙΑ ΤΟΥΣ ΚΑΡΚΙΝΟΥΣ
Ο καρκίνος είναι εξαιρετικά πολύπλοκη πάθηση με μεγάλη ετερογένεια και γι’ αυτό δεν υπάρχει καρκίνος που να είναι ακριβώς ο ίδιος σε διαφορετικούς ανθρώπους. (Στη μεγάλη ετερογένεια του οφείλεται και η διαφορετική ανταπόκριση των ανθρώπων στις θεραπείες.)
Περίπου το 25% των ανθρώπων μετά την αναπαραγωγική ηλικία πεθαίνουν από καρκίνο (αποτελεί τη δεύτερη αιτία θανάτου μετά τα καρδιαγγειακά επεισόδια) και περίπου το 38% των ανθρώπων θα παρουσιάσει καρκίνο στη διάρκεια της ζωής τους.
Η διαδικασία δημιουργίας του καρκίνου περνά συνήθως από πολλά στάδια, διαρκεί πολλά χρόνια, η δε πιθανότητα εμφάνισης του αρχίζει να αυξάνεται στη μέση ηλικία, κορυφώνεται μέχρι την ηλικία των 75 περίπου ετών, οπότε αρχίζει να μειώνεται ελαφρά και σε ηλικίες άνω των 90 ετών παραδόξως η πιθανότητα εμφάνισης του μειώνεται πολύ.
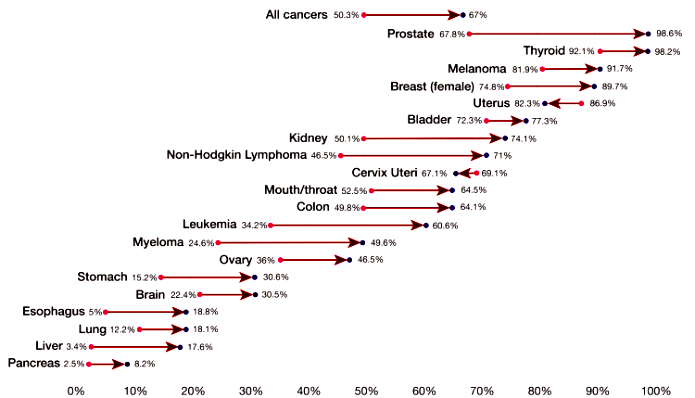
Οι θάνατοι από καρκίνο, μειώθηκαν πρόσφατα (λόγω μείωσης του καπνίσματος στον πληθυσμό, γρηγορότερης διάγνωσης τους και καλύτερης θεραπείας) και η 5ετής επιβίωση για όλους τους καρκίνους συνολικά, έχει αυξηθεί πρόσφατα κοντά στο 70%. (δες πιο κάτω στο κείμενο)
Στο ανωτέρω σχεδιάγραμμα φαίνεται η 5ετής επιβίωση σε διάφορους καρκίνους, από το 2007 ως το 2013 στις ΗΠΑ, συγκριτικά με παλιότερα
>> Ο καρκίνος αναπτύσσεται με πολλούς διαφορετικούς τρόπους από διάφορες αιτίες και το 93%, περίπου των καρκίνων είναι σποραδικοί ή μη κληρονομικοί.
Το υπόλοιπο 7% των καρκίνων είναι οικογενείς, έχουν κληρονομικό υπόβαθρο, εμφανίζονται νωρίτερα στη ζωή και οφείλονται σε μεταλλαγμένα γονίδια που κληρονομούνται από τους γονείς (λιγότερο από το 0.3% του πληθυσμού είναι φορείς γενετικών μεταλλάξεων που ευνοούν τον καρκίνο).
Ο καρκίνος δεν είναι μεταδοτικός, αλλά ορισμένοι ιοί που μπορεί να προκαλέσουν καρκίνο (ογκο-ιοί), είναι μεταδοτικοί μέσω των υγρών του σώματος (π.χ. ο ιός Epstein-Barr (προκαλεί λοιμώδη μονοπυρήνωση), ο ιός της ηπατίτιδας Β και C, ο ιός των ανθρωπίνων θηλωμάτων ή HPV).
[Οι ιοί αυτοί εκτός των άλλων επιδράσεων, διεγείρουν την παραγωγή TERT (τμήμα της Τελομεράσης), που φυσιολογικά είναι απενεργοποιημένη στα σωματικά κύτταρα, έτσι σταθεροποιείται το μήκος των Τελομερών στο ελάχιστο δυνατό, οπότε τα καρκινικά κύτταρα μπορούν να πολλαπλασιάζονται.]
>> Όσα κύτταρα παρουσιάζουν πολλές διαιρέσεις (π.χ. στον μυελό των οστών, στο δέρμα, στο παχύ έντερο) έχουν περισσότερες πιθανότητες να μεταβληθούν σε καρκινικά λόγω αυξημένων πιθανοτήτων για μεταλλάξεις.
ΟΙ ΟΙΚΟΓΕΝΕΙΣ ΚΑΡΚΙΝΟΙ
Τα μεταλλαγμένα γονίδια που κληρονομούνται από τους γονείς είναι κυρίως γονίδια που εμποδίζουν τη δημιουργία όγκου (tumor suppressor genes) ή είναι γονίδια που επιδιορθώνουν το DNA.
[Παραδείγματα κληρονομικών καρκίνων είναι ειδικοί καρκίνοι π.χ. στο μαστό (hereditary breast-ovarian cancer syndrome), στο παχύ έντερο (hereditary non-polyposis colon cancer ή Lynch syndrome) κλπ.
Πάντως κάποια κληρονομικότητα φαίνεται ότι υπάρχει και στους σποραδικούς καρκίνους, όπου αν πρώτου βαθμού συγγενής έχει παρουσιάσει καρκίνο, υπάρχει περίπου 2πλάσια πιθανότητα, συγκριτικά με τους άλλους ανθρώπους, να εμφανιστεί καρκίνος, π.χ. του παχέως εντέρου, του μαστού, του προστάτη κλπ.]
Η ΚΑΤΗΓΟΡΙΟΠΟΙΗΣΗ ΤΩΝ ΚΑΡΚΙΝΩΝ
Οι καρκίνοι μπορούν να κατηγοριοποιηθούν κυρίως βάσει:
α) Του οργάνου ή ιστού που εμφανίζονται,
β) Της εμφάνισης των καρκινικών κυττάρων στο μικροσκόπιο (ιστοπαθολογική- παθολογοανατομική σταδιοποίηση μετά από βιοψία. Tumor grade 1, 2, 3, or 4, ανάλογα με το βαθμό ομοιότητας των καρκινικών κυττάρων με τα φυσιολογικά),
γ) Του μεγέθους και της επέκτασης τους σε λεμφαδένες ή άλλα όργανα (cancer stage / σταδιοποίηση π.χ. με το σύστημα TNM),
δ) Των αλλαγών στα γονίδια που τους προκάλεσαν.
Στην πιο πάνω εικόνα φαίνεται η σταδιοποίηση του καρκίνου του πνεύμονα
ΤΑ ΣΥΜΠΤΩΜΑΤΑ ΤΩΝ ΚΑΡΚΙΝΩΝ
Δυστυχώς τα συμπτώματα του καρκίνου δεν είναι ειδικά (δηλαδή μπορεί να οφείλονται σε πολλές άλλες παθήσεις) και πολλές φορές δεν υπάρχει ο πόνος που οδηγεί στο γιατρό.
Έτσι αν κάποια από τα πιο κάτω ευρήματα ή συμπτώματα επιμένουν πρέπει να οδηγήσουν σε έλεγχο και για καρκίνο:
Αιμορραγίες ή μελανιάσματα χωρίς αιτία, γενικευμένη εξάντληση, πυρετός χωρίς αιτία, νυκτερινοί ιδρώτες, απώλεια ή αύξηση βάρους χωρίς αιτία, δημιουργία θρομβώσεων χωρίς αιτία, ψηλάφηση μάζας π.χ. στο μαστό ή στη μασχάλη, αλλαγές στη θηλή, δυσκολία στην ούρηση, πόνος κατά την ούρηση, κόκκινα ούρα, αλλαγές στις κενώσεις, επίμονος βήχας ή βραχνάδα, δυσπεψία μετά το φαγητό, δυσκολία στην κατάποση, ναυτία- εμετός, πόνος στην κοιλιά, αλλαγές στην όρεξη, αλλαγές στο στόμα, τη γλώσσα, τα χείλη, πονοκέφαλοι, σπασμοί, διαταραχές όρασης ή ακοής, αλλαγές στο δέρμα κλπ.
ΠΟΙΟΣ ΕΧΕΙ ΑΥΞΗΜΕΝΟ ΚΙΝΔΥΝΟ ΓΙΑ ΚΑΡΚΙΝΟ ?
Οι ομάδες με ψηλότερο κίνδυνο καρκίνου είναι: Όσοι είναι μεγάλης ηλικίας, όσοι έχουν ισχυρό οικογενειακό ιστορικό καρκίνου, όσοι έχουν γενετικές μεταλλάξεις που αυξάνουν ορισμένους καρκίνους, όσοι έχουν επαγγελματική έκθεση σε καρκινογόνα (π.χ. Αμίαντο, Χρώμιο, Κάδμιο, βενζόλιο, οξείδιο του αιθυλενίου), όσοι έχουν υποβληθεί σε θεραπευτική ακτινοβολία, όσοι έχουν συμπεριφορές που αυξάνουν τον καρκίνο, όπως το κάπνισμα, η κατανάλωση αλκοόλ, η ηλιοθεραπεία, όσοι έχουν αυξημένο βάρος, όσοι δεν τρώνε πολλά λαχανικά και φρούτα (αψέκαστα), όσοι τρώνε πολύ κρέας ή επεξεργασμένα τρόφιμα κλπ.
ΟΙ ΠΡΟΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΓΙΑ ΚΑΡΚΙΝΟ ΣΤΟ ΓΕΝΙΚΟ ΠΛΗΘΥΣΜΟ
Επειδή τα συμπτώματα του καρκίνου μπορεί να οφείλονται σε πολλές άλλες παθήσεις και επειδή είναι μεγάλης σημασίας η έγκαιρη διάγνωση του, όταν αυτός παραμένει ακόμη εντοπισμένος (οπότε θεραπεύεται πιο εύκολα), διενεργούνται προληπτικές εξετάσεις στο γενικό πληθυσμό.
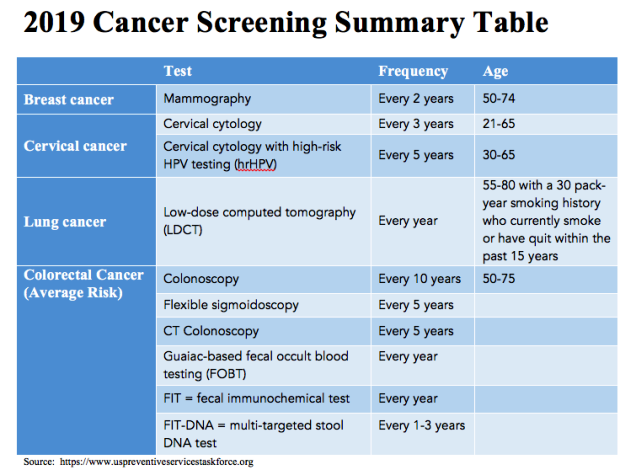
Προληπτικές εξετάσεις στο γενικό πληθυσμό που είναι χρήσιμες για διάγνωση καρκίνου που δεν έχει γίνει αντιληπτός ακόμη, είναι:
Η κολονοσκόπηση μεταξύ 50 και 75 ετών, ο έλεγχος κοπράνων (για αίμα και έλεγχο DNA), η μαστογραφία για γυναίκες 45 ως 75 ετών και η ψηλάφηση του μαστού, το τεστ ΡΑΡ και ο έλεγχος για ιό θηλωμάτων HPV για τον καρκίνο του τραχήλου από ηλικίες 25 ως 75 και η αξονική τομογραφία θώρακος χαμηλής δόσης ακτινοβολίας σε καπνιστές 55 ως 75 ετών.
Άλλες προληπτικές εξετάσεις που πιθανόν να είναι χρήσιμες, ιδίως σε ανθρώπους με αυξημένο κίνδυνο καρκίνου (λαμβάνοντας υπ’ όψιν τα ψευδώς θετικά και τα ψευδώς αρνητικά αποτελέσματα) είναι:
Ο περιοδικός έλεγχος του δέρματος από δερματολόγο, το διακολπικό υπερηχογράφημα σε περιπτώσεις με μετάλλαξη BRCA1 ή BRCA2, η κολονοσκόπηση-γραφία με αξονικό τομογράφο (ή Virtual colonoscopy), η μαγνητική τομογραφία μαστού σε περιπτώσεις με μετάλλαξη BRCA1 ή BRCA2.
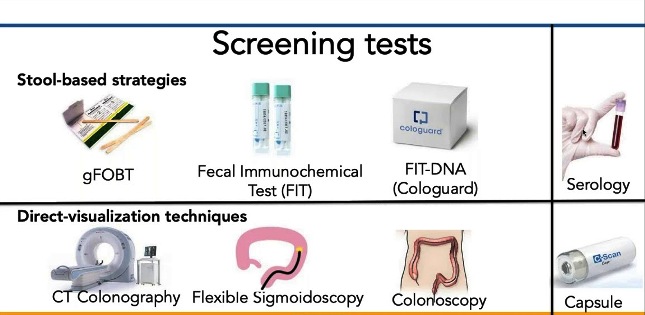
Στην πιο πάνω εικόνα φαίνονται οι προληπτικές εξετάσεις για τον καρκίνο του παχέως εντέρου
Στις πιο πάνω εικόνες φαίνεται κολονοσκόπηση με αξονικό τομογράφο (Virtual colonoscopy)
Επιπλέον άλλες εξετάσεις αίματος που είναι χρήσιμες σε άντρες είναι το PSA μαζί με δακτυλική εξέταση
Πιθανόν είναι χρήσιμες η α-εμβρυϊκή πρωτεΐνη ή Alpha-fetoprotein μαζί με υπερηχογράφημα του ήπατος για ορισμένους με ψηλό κίνδυνο καρκίνου του ήπατος και το CA-125 για καρκίνο ωοθηκών σε γυναίκες με ψηλό κίνδυνο της πάθησης.
https://www.cancer.gov/about-cancer/screening/screening-tests
“ΕΠΑΓΓΕΛΜΑΤΙΚΟΙ” ΚΑΡΚΙΝΟΙ
Οι συχνότεροι καρκίνοι από επαγγελματική έκθεση σε καρκινογόνα είναι του πνεύμονα, της ουροδόχου κύστεως, του δέρματος, οι λευχαιμίες και τα λεμφώματα, το μεσοθηλίωμα, ο ρινοφαρυγγικός.
https://oem.bmj.com/content/75/8/593
> 150 παράγοντες προκαλούν ή πιθανώς προκαλούν καρκίνο και οι 47 από αυτούς είναι γνωστοί επαγγελματικοί καρκινογόνοι παράγοντες [π.χ. Αμίαντος, Χρώμιο, Κάδμιο, βενζόλιο, το οξείδιο του αιθυλενίου (για ιατρική αποστείρωση και αποστείρωση τροφίμων όπως ξηρών καρπών, μπαχαρικών κ.λπ.). κλπ.]
Παραδείγματα επαγγελμάτων με έκθεση σε καρκινογόνα ή πιθανώς καρκινογόνα
υπάρχει στην πιο κάτω διεύθυνση:
https://www.ccohs.ca/oshanswers/diseases/carcinogen_occupation.html
Η ΔΙΑΓΝΩΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ
Η διάγνωση του καρκίνου θα βασιστεί σε ορισμένες εξετάσεις:
α) Στο ιστορικό και στη φυσική εξέταση του ανθρώπου, για οτιδήποτε ασυνήθιστο.
β) Σε εργαστηριακές εξετάσεις αίματος, ούρων, διαφόρων υγρών και ιστών π.χ. οι καρκινικοί δείκτες (tumor markers), η υγρή βιοψία (Liquid biopsie), έλεγχος για μετάλλαξη γονιδίων (π.χ. μετάλλαξη του γονιδίου BRCA1 ή BRCA2 για τον καρκίνο του μαστού και των ωοθηκών), κυτταρολογικές εξετάσεις κλπ. (για ορισμένες εργαστηριακές εξετάσεις δες πιο κάτω),
Υπ’ όψιν ότι δυστυχώς μερικές φορές οι εξετάσεις δεν δείχνουν υπαρκτό καρκίνο (ψευδώς αρνητικές) ή αντίθετα, δείχνουν ψέματα ότι υπάρχει καρκίνος (ψευδώς θετικές).
γ) Σε απεικονιστικές εξετάσεις, όπως η ακτινογραφία, η αξονική τομογραφία, η μαγνητική τομογραφία, το υπερηχογράφημα, ραδιοϊσοτοπικές εξετάσεις, όπως το SPECT ή το PET κλπ., φαίνεται ο καρκίνος και η επέκταση του (σε λεμφαδένες ή άλλα όργανα).
δ) Τελικά η οριστική διάγνωση θα βασιστεί στη βιοψία.
Η ΠΡΟΓΝΩΣΗ ΑΝΘΡΩΠΩΝ ΜΕ ΚΑΡΚΙΝΟ (Η 5ΕΤΗΣ ΕΠΙΒΙΩΣΗ ΤΟΥΣ)
Η πρόγνωση (συνηθίζεται να αναφέρεται σαν 5ετής επιβίωση) διαφέρει ανάλογα με πολλούς παράγοντες, όπως το είδος του καρκίνου (επίσης η ιστοπαθολογική σταδιοποίηση, η ευαισθησία σε ορμόνες, η τυχόν ύπαρξη ορισμένων γονιδιακών μεταλλάξεων), το στάδιο του καρκίνου όταν ξεκίνησε η θεραπεία, την ηλικία, τη γενικότερη υγείας κλπ.
Οι καρκίνοι με τη μεγαλύτερη 5ετή σχετική επιβίωση είναι του μαστού, του προστάτη, του θυρεοειδούς, των όρχεων, το μελάνωμα, του τραχήλου, του Hodgkin λεμφώματος κλπ., ενώ οι καρκίνοι με τη μικρότερη 5ετή σχετική επιβίωση είναι του παγκρέατος, το μεσοθηλίωμα κλπ.
Στην πιο πάνω εικόνα φαίνεται η 5ετής επιβίωση του καρκίνου του προστάτη, ανάλογα με το στάδιο του, όταν αρχίζει η θεραπεία
Η 5ετής επιβίωση εξαρτάται από το είδος και το στάδιο του καρκίνου κατά την έναρξη της θεραπείας (συμπεριλαμβανομένης και της χημειοθεραπείας) και υπολογίζεται σαν μέσος όρος όλων των ηλικιών, της υπόλοιπης υγείας, και της δραστικότητας του ανοσοποιητικού συστήματος του κάθε ανθρώπου με καρκίνο.
Έτσι ο μέσος όρος της 5ετούς επιβίωσης είναι ανάλογος του σταδίου (της επέκτασης) του κάθε διαφορετικού καρκίνου και συνεπώς του σταδίου του όταν ξεκίνησε η θεραπεία του.
Ο πρώτος αριθμός αφορά εντοπισμένο καρκίνο στο όργανο που εμφανίστηκε (Localized), ο δεύτερος αριθμός αφορά τοπική μόνο επέκταση του σε λεμφαδένες και ιστούς (Regional, κυρίως σταδίου III) και ο τρίτος αριθμός αφορά μετάσταση σε μακρινά όργανα (Distant, σταδίου IV):
Για τον καρκίνο του θυρεοειδούς (Papillary) η 5ετής επιβίωση είναι: 99% – 97% – 78%.
Για τον καρκίνο του προστάτη: 99% – 97% – 30%.
Για τον καρκίνο του μαστού: 99% – 85% – 26%.
Για τον καρκίνο των όρχεων: 99% – 96% – 74%.
Για τον καρκίνο της μήτρας: 95% -68%- 17%.
Για το μελάνωμα: 98% – 64% – 23%.
Για τον καρκίνο του παχέως εντέρου: 90% – 71% – 13%.
Για τον καρκίνο του νεφρού: 93% – 69% – 12%.
Για το μη Hodgkin λέμφωμα (large B-cell): 72% – 72% – 55%.
Για τον καρκίνο του Λάρυγγα (Glottis): 83% – 50% – 42%.
Για τον καρκίνο της ουροδόχου κύστεως: 70% – 34% – 5%.
Για τον καρκίνο του στομάχου: 68% – 31% – 5%.
Για τον καρκίνο του πνεύμονα: 57% – 27% – 4%.
Για τον καρκίνο του οισοφάγου: 45% – 24% – 5%.
Για τον καρκίνο του παγκρέατος: 34% – 12% – 3%.
Για τον καρκίνο του ήπατος: 31%- 11%- 2%.
Υπ’ όψιν ότι αυτά τα ποσοστά δεν λαμβάνουν υπ’ όψιν τις τελευταίες εξελίξεις στη θεραπεία, γιατί δείχνουν στατιστικές προηγούμενων χρόνων (μέχρι το 2013-14).
https://www.cancer.org/cancer/kidney-cancer/detection-diagnosis-staging/survival-rates.html
https://www.medicalnewstoday.com/articles/326031.php
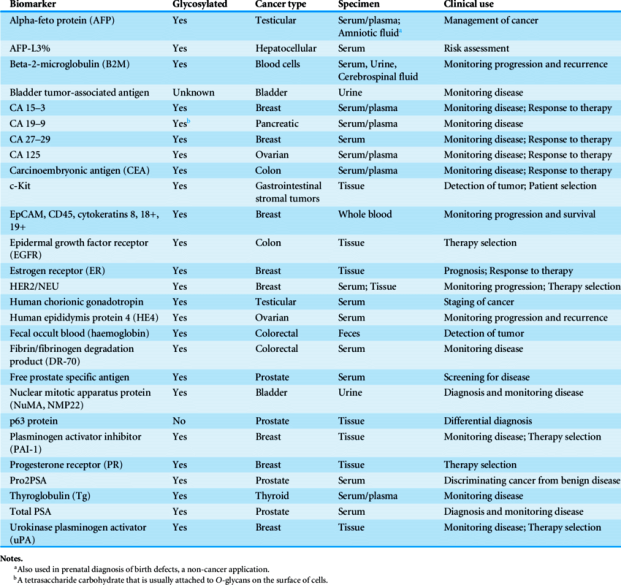
ΕΡΓΑΣΗΡΙΑΚΕΣ ΕΞΕΤΑΣΕΙΣ – ΟΙ ΚΑΡΚΙΝΙΚΟΙ ΔΕΙΚΤΕΣ
Αυτοί είναι ουσίες (πρωτεΐνες, γονίδια κλπ.) που εκκρίνονται είτε από τα καρκινικά κύτταρα είτε από άλλα κύτταρα, σαν αντίδραση στον καρκίνο.
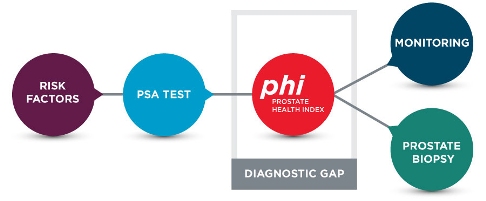
ΤΟ PSA
Το γνωστό PSA (πρωτεΐνη-ένζυμο) δυστυχώς δεν είναι ακριβές για τη διάγνωση του καρκίνου του προστάτη. Σε άντρες με τιμές κάτω από 4 ng/mL μπορεί να υπάρχει καρκίνος, ενώ σε τιμές πάνω από 4 ng/mL μπορεί να μην υπάρχει καρκίνος. Σε τιμές 4 ως 10 ng/mL, μόνο η μια στις 3 βιοψίες δείχνει καρκίνο. Δες το άρθρο για το PSA.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5895603/
Άλλα παραδείγματα καρκινικών δεικτών που κυκλοφορούν κυρίως στο αίμα και χρησιμοποιούνται για έλεγχο ανταπόκρισης στη θεραπεία είναι: Η Καλσιτονίνη (calcitonin) για το μυελώδη καρκίνο του Θυρεοειδούς, το CA-125 για τον καρκίνο των ωοθηκών, η β2 μικροσφαιρίνη (beta-2-microglobulin) για μερικά λεμφώματα, το πολλαπλούν μυέλωμα και τη χρόνια λεμφοκυτταρική λευχαιμία.
ΕΛΕΓΧΟΣ ΓΙΑ ΜΕΤΑΛΛΑΞΗ ΓΟΝΙΔΙΩΝ ΚΑΡΚΙΝΙΚΩΝ ΚΥΤΤΑΡΩΝ
Με τον έλεγχο πιθανής μετάλλαξης ανιχνεύεται αν ορισμένα γονίδια είναι μεταλλαγμένα, ώστε να δοθεί η κατάλληλη θεραπεία σε συγκεκριμένους καρκίνους, π.χ. το γονίδιο EGFR σε μη μικροκυτταρικό καρκίνο του πνεύμονα, το γονίδιο BRAF σε καρκίνο παχέως εντέρου και σε μελάνωμα.
Επίσης ελέγχεται αν το γονίδιο ERBB2 ‘’υπερλειτουργεί’’ ή είναι αυξημένη η πρωτεΐνη-υποδοχέας του, HER2/neu (ή HER2), σε καρκίνο του μαστού και άλλους καρκίνους, για να δοθεί η κατάλληλη θεραπεία.
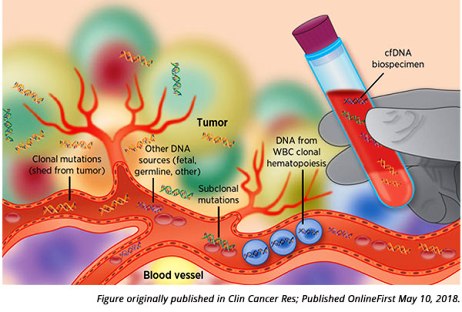
Η ΥΓΡΗ ΒΙΟΨΙΑ
Η υγρή βιοψία (Liquid biopsie) αφορά την ανίχνευση μορίων του καρκινικού κυττάρου (π.χ. τμημάτων DNA) ή και ολόκληρων καρκινικών κυττάρων στο αίμα και σε άλλα υγρά.
Όταν τα καρκινικά κύτταρα πεθαίνουν, τα κομμάτια τους συμπεριλαμβανομένων και κομματιών από το DNA τους (circulating tumor DNA/ct DNA) κυκλοφορούν στο αίμα και αποβάλλονται στα ούρα.
Η υγρή βιοψία προς το παρόν χρησιμοποιείται μόνο για ορισμένους τύπους καρκίνου ώστε να δοθεί η κατάλληλη ανοσοθεραπεία ή στοχευμένη θεραπεία, ανάλογα με τις μεταλλάξεις που τον δημιούργησαν ή για να ανακαλυφθούν υποτροπές τους.
Οι μεταλλάξεις που δημιούργησαν τον καρκίνο ανιχνεύονται με το Next Generation Sequencing ή NGS (αυτό ανιχνεύει πολλές μεταλλάξεις ταυτόχρονα, με μια μόνο εξέταση) των ct DNA.
Το FDA έχει εγκρίνει το Cobas Liquid biopsie test για ανίχνευση μετάλλαξης στο γονίδιο EGFR σε ορισμένους ασθενείς με καρκίνο του πνεύμονα και ετοιμάζεται να εγκρίνει ορισμένα άλλα (π.χ. το Foundation One® Liquid ή το Guardant360®, Signatera™).
https://ascopubs.org/doi/full/10.1200/JCO.2017.76.8671
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6299472/
https://www.cancer.gov/about-cancer/diagnosis-staging/diagnosis/tumor-markers-fact-sheet
https://onlinelibrary.wiley.com/doi/full/10.1111/apm.12912
ΟΙ ΜΗΧΑΝΙΣΜΟΙ ΔΗΜΙΟΥΡΓΙΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ (ΜΕ ΜΕΓΑΛΥΤΕΡΗ ΛΕΠΤΟΜΕΡΕΙΑ)
Το σώμα μας διατηρείται για πολλά χρόνια ζωντανό, χάρη στην ανανέωση των κυττάρων των ιστών με τις κυτταρικές διαιρέσεις που συμβαίνουν περίπου 40-70 φορές στη διάρκεια της ζωής του ενήλικου ανθρώπου.
Σχεδόν όλα τα κύτταρα στο σώμα μας ανανεώνονται συνεχώς (γιατί γερνούν και πεθαίνουν), είτε μέσω διαιρέσεων τους (μίτωση) είτε από τα σωματικά βλαστοκύτταρα, ανάλογα με τον ιστό που βρίσκονται και ανάλογα με τις συνθήκες.
Στις κυτταρικές διαιρέσεις μεταφέρεται ακριβώς το ίδιο, αρχικό, γονιδιακό υλικό (DNA) του πρώτου κυττάρου (ζυγώτη) από τη μια γενιά κυττάρων στις επόμενες γενιές.
Όσα κύτταρα διαιρούνται έχουν διάφορες φάσεις στη ζωή τους (κυτταρικός κύκλος), όπου κάθε φορά διπλασιάζεται το DNA (στα χρωματοσώματα) και τα υπόλοιπα οργανίδια ώστε να καταλήξουν σε δύο πανομοιότυπα θυγατρικά κύτταρα (μίτωση).
Για να διασφαλιστεί ότι δεν θα δημιουργηθεί λάθος στην αντιγραφή του DNA, υπάρχουν σημεία ελέγχου στη φάση του δημιουργίας 2 θυγατρικών κυττάρων. Αυτά είναι 3, το checkpoint 1, 2 και 3 (Metaphase checkpoint)
Ελέγχεται δηλαδή αν το DNA έχει αναπαραχθεί ακριβώς, χωρίς καμιά βλάβη σ’ αυτό και αν το περιβάλλον του κυττάρου είναι ευνοϊκό (σε θρεπτικά στοιχεία και με επαρκή χώρο) για τη δημιουργία 2 θυγατρικών κυττάρων.
>> Όσο περισσότερες διαιρέσεις υφίστανται τα ενήλικα σωματικά κύτταρα, τόσο περισσότερες μεταλλάξεις αθροίζονται σ’ αυτά, οπότε αυξάνεται ο κίνδυνος καρκίνου.
Υπ’ όψιν ότι κάθε φορά που τα κύτταρα διαιρούνται, οι προστατευτικές άκρες των χρωματοσωμάτων, που λέγονται τελομερή, καταστρέφονται μερικώς για να μην καταστραφεί το χρήσιμο DNA.
Οπότε κάποια στιγμή, μετά από περίπου 40- 70 διαιρέσεις, μικραίνουν τόσο πολύ τα τελομερή, που το κύτταρο σταματά να διαιρείται (μπαίνει σε φάση G 0), ώστε να μην καταστραφεί το χρήσιμο DNA του χρωματοσώματος.
>> Το πρώτο καρκινικό κύτταρο έχει καταφέρει να ξεφύγει διαδοχικά και πολλά στάδια, από όλους τους ελέγχους και επιδιορθώσεις του DNA, όπως και από τον προγραμματισμένο θάνατο (απόπτωση) και αρχίζει να διαιρείται κυρίως μέσω αύξησης της τελομεράσης (ή στο 10% από άλλους μηχανισμούς “επιμήκυνσης” των τελομερών, που λέγονται ALT).
Για τη δημιουργία του καρκινικού κυττάρου είναι απαραίτητες:
Α) Αρχικά οι κατάλληλες μεταλλάξεις σε πολλά γονίδια που ευνοούν τον καρκίνο ή/και οι επιγενετικές αλλαγές, που ενεργοποιούν ή απενεργοποιούν γονίδια που ευνοούν τον καρκίνο.
1) Τα γονίδια που ευνοούν τον καρκίνο και που ΑΥΞΑΝΕΤΑΙ η δράση τους (π.χ. ras family of genes και HER2) είναι τα ογκογονίδια (ongogenes). Αυτά αυξάνουν τις κυτταρικές διαιρέσεις και εμποδίζουν την απόπτωση (προγραμματισμένο θάνατο) σε όσα κύτταρα έχουν βλάβες του DNA που είναι αδύνατον να διορθωθούν.
Η δράση τους αυξάνεται μέσω μεταλλάξεων ή μέσω επιγενετικών μηχανισμών (π.χ. από ακετυλίωση Ιστονών).
2) Τα γονίδια που ευνοούν τον καρκίνο και ΜΕΙΩΝΕΤΑΙ η “δράση” τους (π.χ. p53, BRCA1, and BRCA2) μέσω μεταλλάξεων ή επιγενετικών μηχανισμών (π.χ. από μεθυλίωση του DNA) είναι:
i) τα γονίδια που καταπιέζουν τη δημιουργία όγκων (Tumor–suppressor genes)
(Τα Tumor-suppressor genes εμποδίζουν τις κυτταρικές διαιρέσεις και ευνοούν την απόπτωση στα κύτταρα με αδιόρθωτες βλάβες του DNA).
ii) τα γονίδια που προκαλούν διόρθωση του DNA.
Έτσι αν μειωθεί η δράση των Tumor-suppressor genes [π.χ. τα γονίδια για τις πρωτεΐνες p53 και p16/Rb (Retinoblastoma protein)], αυξάνονται οι κυτταρικές διαιρέσεις και τα κύτταρα δεν υφίστανται προγραμματισμένο θάνατο.
[Τα γονίδια που καταπιέζουν τη δημιουργία όγκων για να δραστηριοποιηθούν θα χρειαστεί να μεταλλαχθούν και τα δύο γονίδια του ζεύγους, ενώ τα ογκογονίδια ενεργοποιούνται με μετάλλαξη μόνο του ενός από τα δυο του ζεύγους]
Β) Στη συνέχεια αφού επιβιώσουν από το θάνατο, το πρώτο-πρώτα καρκινικά κύτταρα πρέπει να αρχίσουν να διαιρούνται. Για να το καταφέρουν πρέπει να διατηρήσουν το μήκος των τελομερών τους στο ελάχιστο δυνατό για να μπορούν να συνεχίζουν τις διαιρέσεις, οπότε γίνονται “αθάνατα” (με αμέτρητες διαιρέσεις) καρκινικά κύτταρα.
Η διατήρηση στο ελάχιστο δυνατό του μήκους των τελομερών γίνεται κυρίως μέσω της δημιουργίας τελομεράσης, στο 85-90% των περιπτώσεων και με άλλους μηχανισμούς επιμήκυνσης, που λέγονται ALT, στο υπόλοιπο 10-15% των περιπτώσεων).
# Έτσι περίπου στο 90% των καρκίνων τα κύτταρα πολλαπλασιάζονται ανεξέλεγκτα λόγω της έκφρασης (δημιουργίας) τελομεράσης κυρίως λόγω της ενεργοποίησης του γονιδίου TERT (από μεταλλάξεις ή επιγενετικούς μηχανισμούς).
[Το γονίδιο TERT κανονικά είναι σιωπηλό (δεν δημιουργεί mRNA) σχεδόν σε όλα τα σωματικά κύτταρα (εκτός από τα σωματικά stem cells/progenitor cells και τα ενεργοποιημένα λεμφοκύτταρα).
Μέσω του μηχανισμού της τελομεράσης δημιουργείται κυρίως το μελάνωμα, το γλοίωμα (και ιδίως το γλοιοβλάστωμα), ο καρκίνος της ουροδόχου κύστης, το ηπατοκυτταρικό καρκίνωμα κλπ.]
# Περίπου στο 10% των καρκίνων τα τελομερή, έχουν άλλους μηχανισμούς διατήρησης του μήκους τους που λέγονται ALT (Αlternative Lengthening of Τelomeres), όπου συμβαίνει ανασυνδυασμός DNA (ανεξάρτητα από την ύπαρξη τελομεράσης).
[Μέσω των μηχανισμών ALT δημιουργούνται οι καρκίνοι του συνδετικού ιστού (μεσεγχυματικοί) και είναι τα σαρκώματα των οστών και των μαλακών μορίων (π.χ. των μυών κλπ).]
Γ) Όταν ο συμπαγής καρκίνος φτάσει σε κάποιο μέγεθος, πρέπει να δημιουργήσει νέα αγγεία για να μπορέσουν να ζήσουν τα νέα καρκινικά κύτταρα. Έτσι ορισμένα γονίδια δημιουργούν νέα μικρά αγγεία από προϋπάρχοντα αγγεία.
Δ) Επιπλέον τα καρκινικά κύτταρα πρέπει να καταφέρουν να μην δέχονται επιθέσεις από το ανοσοποιητικό σύστημα και το επιτυγχάνουν με διάφορες στρατηγικές, π.χ. μέσω μείωσης των αντιγόνων ιστοσυμβατότητας στην επιφάνεια τους (Major Histocompatibility Complex-1 ή MHC-1) για να μην έχουν “ξένη” καρκινική πρωτεΐνη στην επιφάνεια τους που θα αναγνωρίσουν και εξοντώσουν τα CD8+ T λεμφοκύτταρα).
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5138279/
https://www.frontiersin.org/articles/10.3389/fgene.2019.00079/full
https://link.springer.com/article/10.1007/s12272-019-01126-z
ΤΑ ONCOMIRS
Δυστυχώς, τα πράγματα είναι ακόμη πιο πολύπλοκα, έτσι πέρα από τους πιο πάνω μηχανισμούς που ευνοούν τη δημιουργία καρκίνου, υπάρχουν και συγκεκριμένα miRNAs που ευνοούν τη δημιουργία καρκίνου.
Τα miRNAs είναι μικρά, περίπου με 22 νουκλεοτίδια (noncoding) RNAs, που μειώνουν την παραγωγή πρωτεΐνης (μετάφραση) από κάποιο γονίδιο καταστρέφοντας το mRNA του γονιδίου αυτού.
Έτσι ορισμένα microRNAs που λέγονται oncomiRs (π.χ. miR221/222, miR155, miR 15-21, miR-135), όταν αυξηθεί η έκφρασης τους (η “ποσότητα” τους) μέσω μεταλλάξεων ή επιγενετικών μεταβολών, αυξάνουν την καρκινογένεση, γιατί μειώνουν τις πρωτεΐνες από: 1) τα tumor suppressor genes, 2) τα γονίδια που προκαλούν διόρθωση του DNA και 3) τα γονίδια που προκαλούν απόπτωση.
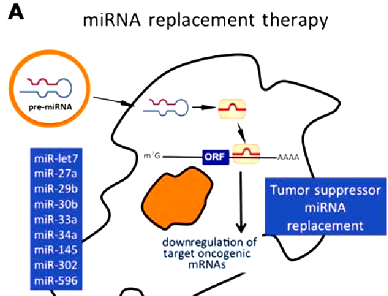
Υπάρχουν όμως και ορισμένα microRNAs, που ονομάζονται tumor suppressor miRs που μειώνουν τη δημιουργία πρωτεϊνών από τα ογκογονίδια, έτσι όταν αυξηθεί η έκφραση τους (η “ποσότητα” τους), μειώνεται η καρκινογένεση (π.χ. miR-506, miR let7, miR-143, miR-145, mir-34, miR-200)
Τα miRNAs είναι υποσχόμενα σαν μελλοντική εξέταση για έγκαιρη διάγνωση καρκίνων και για παρακολούθηση της θεραπείας τους.
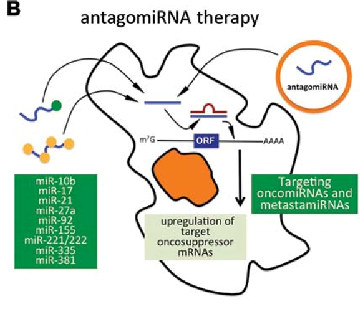
Επιπλέον η αναστολή των oncomiRs (με ASO) και η αύξηση της δράσης των tumor suppressor miRs (TS-miR) (εισαγωγή συνθετικού miRNA που μιμείται τη δράση του TS-miR), μπορεί να οδηγήσει σε νέες θεραπείες του καρκίνου.
https://www.nature.com/articles/s10038-021-00938-6
https://www.spandidos-publications.com/ijo/49/1/5
https://clinicalepigeneticsjournal.biomedcentral.com/articles/10.1186/s13148-018-0587-8
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6447849/
https://www.frontiersin.org/articles/10.3389/fgene.2019.00626/full
ΟΙ ΒΛΑΒΕΣ ΤΟΥ DNA ΚΑΙ Η ΔΗΜΙΟΥΡΓΙΑ ΚΑΡΚΙΝΟΥ
Το DNA μας υφίσταται συνεχείς βλάβες τόσο από ΕΝΔΟΓΕΝΕΙΣ παράγοντες (π.χ. από λάθη αντιγραφής του DNA) όσο και από ΕΞΩΓΕΝΕΙΣ παράγοντες (π.χ. το κάπνισμα, η υπεριώδης ηλιακή ακτινοβολία, άλλα είδη ακτινοβολίας, ορισμένες τοξίνες, ορισμένες χημικές αρωματικές ουσίες όπως το βενζόλιο και το τολουένιο, από ιώσεις κλπ.).
Οι βλάβες του DNA κατά την αντιγραφή του μπορεί να προκαλέσουν μετάλλαξη γονιδίων και αν το γονίδιο που έχει υποστεί τη μόνιμη βλάβη, είναι γονίδιο που εμποδίζει τη δημιουργία καρκίνου π.χ. γονίδιο που εμποδίζει τη δημιουργία όγκου (π.χ. το γονίδιο της πρωτεΐνης p53), γονίδιο που επιδιορθώνει το DNA ή είναι γονίδιο που λόγω μετάλλαξης έγινε γονίδιο που ευνοεί τον καρκίνο (ογκογονίδιο), τότε αυξάνεται η πιθανότητα δημιουργίας καρκίνου.
Οι βλάβες του DNA μπορεί να είναι αλλαγή ή απώλεια νουκλεοτιδίου- βάσης, “σπάσιμο” της μιας ή και των δυο ελίκων του.
Για να διορθωθούν οι βλάβες του DNA, το κύτταρο έχει αναπτύξει μηχανισμούς (κατά τη διάρκεια της εξέλιξης), που τις ανιχνεύουν και τις επιδιορθώνουν. Αυτοί λέγονται μηχανισμοί DDR (DNA Damage Response) και αποτελούνται από ομάδα ειδικών πρωτεϊνών.
Αν ο ρυθμός των βλαβών του DNA είναι μεγαλύτερος από το ρυθμό της επιδιόρθωσης τους, ή αν το γονίδιο του DNA που έχει υποστεί τη μόνιμη βλάβη, είναι σημαντικό γονίδιο (π.χ. γονίδιο που εμποδίζει τη δημιουργία όγκου, ή γονίδιο που επιδιορθώνει το DNA), οι βλάβες στο DNA συσσωρεύονται, οπότε το κύτταρο μπορεί να γίνει καρκινικό [ή να μπει σε φάση γήρανσης ή προγραμματισμένου θανάτου (απόπτωση)].
Πολύ σπάνια, μερικά κύτταρα (περίπου 1 στις 1.000.000 διαιρέσεις κυττάρων) καταφέρνουν να ξεφύγουν από τη γήρανση και το θάνατο, με σταθεροποίηση του μήκους των τελομερών τους στο ελάχιστο δυνατό, οπότε μπορούν να πολλαπλασιάζονται διαρκώς και ανεξέλεγκτα (“αθάνατα” – καρκινικά κύτταρα).
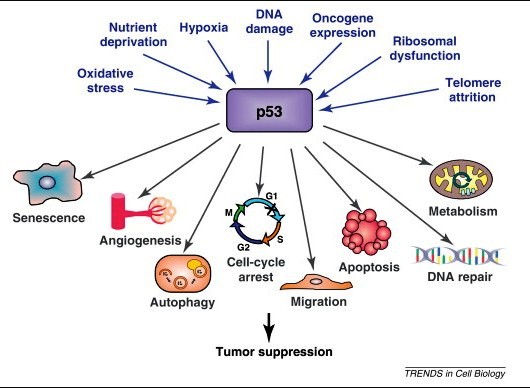
Φυσιολογικά σε βλάβη του DNA αυξάνεται η πρωτεΐνη p53, που σταματά τον κυτταρικό κύκλο και επιστρατεύει διάφορα ένζυμα για να το επιδιορθώσουν. Αν δεν είναι εφικτή η επιδιόρθωση του DNA, η p53 προκαλεί απόπτωση (θάνατο) ή γήρανση λειτουργιών (senescence) του κυττάρου.
Αν όμως μεταλλαχθεί το γονίδιο της πρωτεΐνης tp53, έχουμε απώλεια της λειτουργικότητας της, δεν επιδιορθώνεται το DNA μέσω των μηχανισμών DDR, οπότε γίνεται επιτρεπτό να δημιουργηθεί ο καρκίνος.
Στους καρκίνους το συχνότερα μεταλλαγμένο γονίδιο είναι αυτό που προκαλεί τη δημιουργία (εκφράζει) την πρωτεΐνη p53.
ΕΝΔΕΙΚΤΙΚΗ ΒΙΒΛΙΟΓΡΑΦΙΑ
https://www.cancer.gov/about-cancer
(Στην πιο κάτω εικόνα φαίνονται Τ λεμφοκύτταρα, με πορτοκαλί χρώμα, που επιτίθενται σε καρκινικό κύτταρο)